王宏伟研究组在Nature子刊发表文章报道RNA干扰及相关蛋白质因子调节的结构机制
2013年4月28日,生命中心王宏伟研究组在《Nature》子刊《Nature Structural and Molecular Biology》在线发表题为“Substrate-specific structural rearrangements of human Dicer”的研究论文,报道了在RNA干扰(RNAi)通路中人源Dicer蛋白加工小RNA的活性受RNA前体自身结构及相关蛋白质因子调节的结构机制。
RNA干扰及相关的RNA介导的基因沉默通路是真核生物细胞中的重要基因调控机制之一。在该基因调控通路中,装载在RNA沉默诱导复合体中的小RNA分子(包括siRNA和miRNA)通过与标靶信使RNA的序列匹配来特异性地抑制信使RNA的翻译,从而导致基因表达沉默。小RNA分子是由细胞核内或者外源的较长的双链RNA被特异性的RNA酶Dicer蛋白切割后所生成。在人体内只有一种Dicer蛋白,它同时负责对siRNA和miRNA的加工。已有的研究表明,人源Dicer对miRNA前体的加工效率远远大于对siRNA前体的加工。理解该现象的机理对于深入认识RNAi的调控机制及设计更有效的RNAi前体分子具有重要意义。但是到目前为止,尚无任何对该过程分子机制的解释。
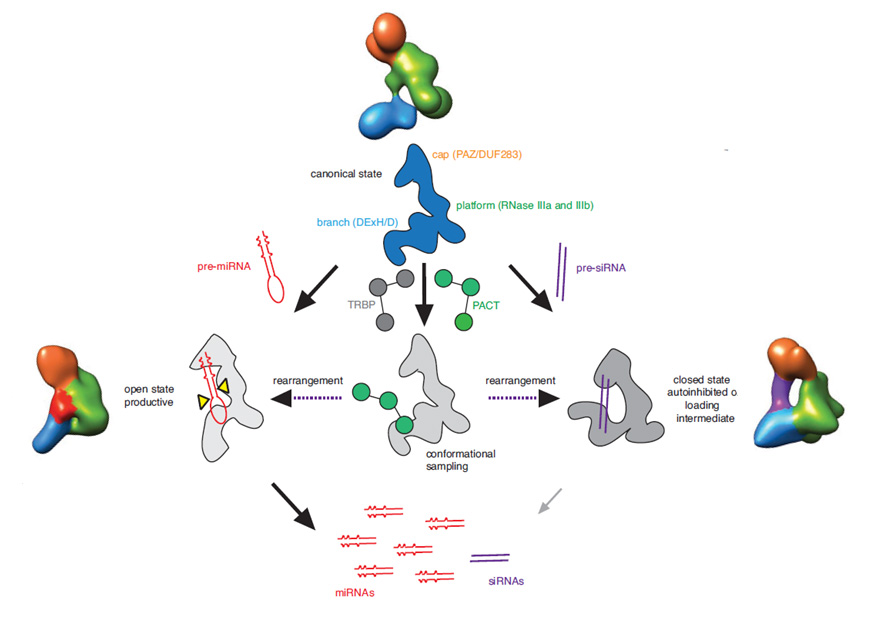
利用电子显微学和单颗粒计算机三维重构技术,王宏伟及合作者们首次获得了人源Dicer蛋白及其与多种小RNA前体复合体的冷冻电子显微镜结构,发现了siRNA前体及miRNA前体的不同结构导致它们诱导人源Dicer产生不同的构象变化,从而导致前者难以接近而后者很容易到达Dicer的酶活位点。这个发现首次为人源Dicer切割不同RNA底物活性的差异提出了分子机制上的解释。更进一步,该论文还发现调节小RNA生成的蛋白质TRBP及PACT都诱导Dicer的构象变化,使其适于切割小RNA前体,从而促进小RNA的生成。
该工作是王宏伟自2009年在同一刊物上发表RNAi通路中RISC-loading complex的电子显微学三维重构后对这一系统研究的后续成果。该成果是与美国及日本的另外两个研究小组共同合作完成,王宏伟为论文通讯作者。目前在国家自然科学基金委的支持下,王宏伟研究组利用清华大学生命学院的冷冻电子显微学平台,正在继续深入这一领域的研究工作。