药物性肝损伤是新药研发和临床用药安全中长期存在的重要挑战。其中,相较于药物直接作用于肝细胞所造成的“直接性肝毒性”,由细胞间通讯失衡、炎症调控异常或微环境改变所驱动的“间接性肝毒性”更难识别,其机制也长期缺乏合适的人源化模型进行系统研究。如何在体外更真实地重建肝脏复杂细胞生态,并识别这类隐匿的毒性风险,一直是药物安全评价领域关注的关键问题。
近日,生命中心/清华大学生物医学工程学院杜亚楠教授团队与合作者在 Nature Communications 发表题为 “Multi-lineage hepatic organoids reveal toxic exosome mediated indirect hepatotoxicity” 的研究论文。研究团队构建了由人胚胎干细胞分化而来的五细胞谱系三维肝类器官,系统整合肝细胞、胆管细胞、肝星状细胞、内皮细胞和库普弗细胞,建立了更接近人体肝脏微环境的药物毒性评估平台。借助这一平台,团队不仅实现了对药物性肝损伤更高保真度的识别,还发现抗抑郁药丙咪嗪(Imipramine,IMP)可通过诱导肝星状细胞释放“毒性外泌体”,进而造成肝细胞凋亡,揭示了间接性肝毒性的全新机制。

构建多谱系肝类器官,建立更仿生的药物肝毒性评估平台
研究中,团队从人胚胎干细胞出发,定向分化获得五类关键肝脏细胞,并按接近生理比例组装为三维多谱系肝类器官(3D MLHOs)。该模型在转录组层面与人肝组织具有更高相似性,在药物代谢、白蛋白分泌、尿素合成、糖脂代谢以及炎症应答等方面,也明显优于传统二维肝细胞培养和仅含肝细胞的三维球体模型,显示出更强的生理仿真能力。进一步地,研究团队利用该平台对58种临床药物进行了系统筛查。结果显示,这一多谱系肝类器官模型对已知肝毒性药物具有较高识别能力,整体预测灵敏度达82.4%,特异性达75%。与传统仅含肝细胞的模型相比,该平台尤其擅长发现依赖细胞间相互作用而产生的毒性效应,为识别“看不见”的间接性肝毒性提供了有力工具。
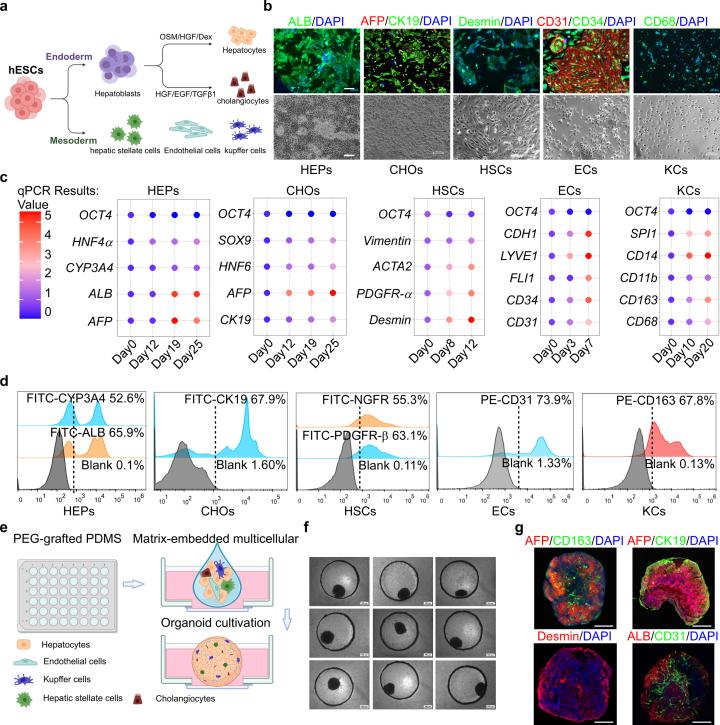
人胚胎干细胞分化五种肝细胞及类器官(3D MLHOs)的构建
多谱系肝类器官揭示传统体系难识别的间接性肝毒性
在药物筛查过程中,研究团队发现,多谱系肝类器官能够识别出一类在单一肝细胞模型中不易显现的损伤模式。这类损伤并非主要来自药物对肝细胞的直接打击,而更依赖于肝脏非实质细胞的参与及其与肝细胞之间的相互作用,提示模型具备解析“间接肝毒性”的独特优势。
基于这一发现,团队进一步结合单细胞数据分析、细胞共培养和条件培养液实验,锁定了肝星状细胞在该类损伤中的关键作用。研究表明,肝星状细胞来源的外泌体可对肝细胞造成显著继发损伤,提示非实质细胞介导的跨细胞通讯失衡,是复杂肝毒性发生的重要环节。这一结果进一步证明,多谱系肝类器官不仅能“发现毒性”,还能帮助定位传统模型难以解析的关键致损细胞与作用路径。
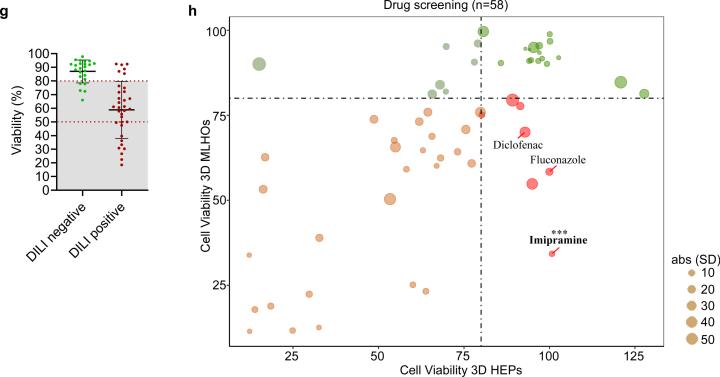
多谱系肝类器官对58种临床来源肝毒性药物进行筛选
毒性外泌体介导细胞间通讯失衡,驱动肝细胞凋亡
围绕这一发现,研究团队进一步解析了分子机制。结果表明,Imipramine作用于肝星状细胞后,可激活p53/hnRNPA2B1/DGCR8信号轴,促使miR-34a-3p被选择性富集到肝星状细胞分泌的外泌体中。这些外泌体随后被肝细胞摄取,将 miR-34a-3p 递送至受体细胞内,并抑制抗凋亡分子XIAP表达,最终激活 caspase-3 通路,引发肝细胞凋亡。
值得注意的是,研究显示Imipramine处理并未明显增加外泌体总量或粒径变化,真正决定其毒性的不是“外泌体释放更多了”,而是“外泌体装载的内容变质了”。也就是说,肝星状细胞在药物刺激下将正常外泌体转变为携带异常miRNA货载的“毒性外泌体(Toxic-EXOs)”,由此介导对肝细胞的远程损伤。这一结果将药物性肝损伤研究的重点,从单一细胞毒性评价推进到了细胞间通讯失衡层面。
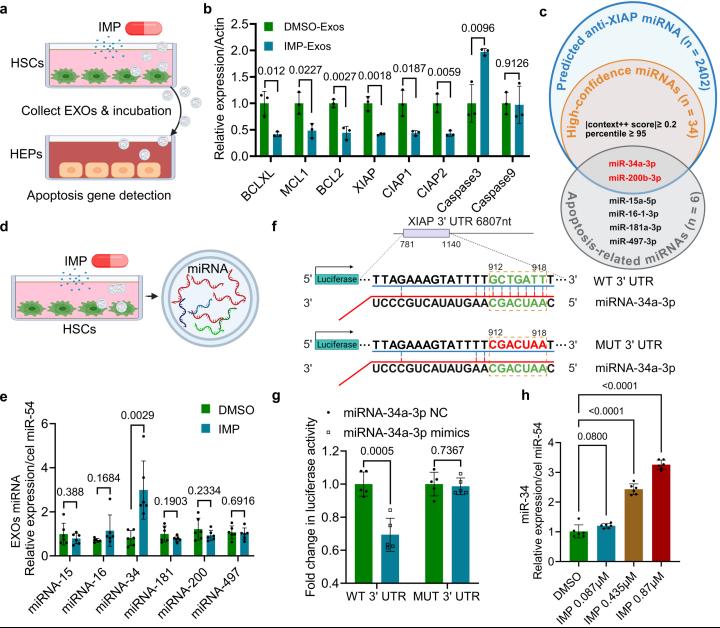
肝星状细胞释放装载miR-34的“毒性外泌体”
为药物安全评价和干预策略开发提供新方向
长期以来,间接肝毒性因机制复杂、模型缺失而难以系统研究。此次工作构建的人源多谱系肝类器官平台,将肝实质细胞与多类非实质细胞纳入同一三维微环境,为研究复杂药物反应提供了更接近人体真实状态的实验系统。研究不仅展示了该模型在复杂肝毒性识别中的优势,也证明其能够进一步解析跨细胞通讯介导的致损机制。
这项研究建立了一套可用于复杂肝毒性评估、机制研究和潜在干预策略探索的原创平台。未来,该模型有望应用于更多药物安全性评价场景,并为人源化肝脏疾病模型的构建提供新思路。
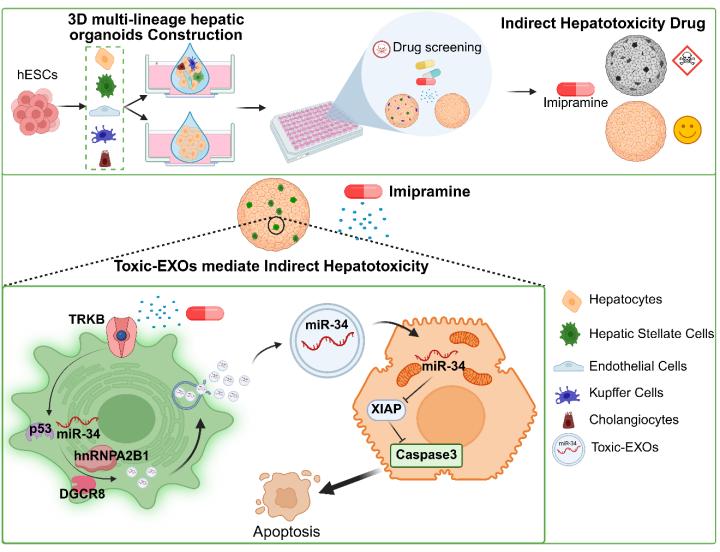
多谱系肝类器官揭示“毒性外泌体”跨细胞毒性机制示意图
清华大学生物医学工程学院原博士后孙雷(现为北京中医药大学中医学院副教授)为论文第一作者,清华-北大生命联合中心研究员、清华大学生物医学工程学院教授杜亚楠和北京大学302临床医学院主任医师曾珍为共同通讯作者,清华大学生物医学工程学院博士生张钰莹、牛宇迪、周律、陈羿翰、刘志强、王天天、梁恺倪、樊东东、首都医科大学宣武医院杨鹤博士、南方医科大学贾晓东博士对本研究有重要贡献。本研究得到了国家自然科学基金、北京市自然科学基金、北京中医药大学中央高校基本科研业务费专项资金的资助。
原文链接:
https://www.nature.com/articles/s41467-026-69548-0
