IgG是血浆中含量最丰富的抗体,在囊膜病毒的识别、中和、免疫清除方面发挥关键作用。IgG抗体拥有两个识别抗原的Fab结构域,可如同双手协同一般同时结合两个抗原表位。这种二价结合能显著提升抗体对抗原的结合强度,该效应被称为亲合力(avidity)。与表征单点结合强度的亲和力(affinity)不同,亲合力反映了抗体多位点协同作战的整体结合能力,威力远胜单价结合的简单叠加。
IgG的亲合力效应可以有效提升对新冠病毒、流感病毒、呼吸道合胞病毒、中东呼吸综合征病毒、基孔肯雅病毒、登革病毒等多种囊膜病毒的中和效率。但长期以来,受IgG分子自身柔性与囊膜病毒天然多形性的制约,既往X射线晶体学及单颗粒冷冻电子显微镜研究通常仅聚焦于Fab片段与病毒糖蛋白胞外段的结合,始终无法看清IgG抗体如何在真实囊膜病毒表面实现二价结合。
2026年4月11日,生命中心/清华大学生命学院李赛课题组在《自然通讯》(Nature Communications)在线发表题为“冷冻电子断层成像解析新冠病毒IgG二价结合并揭示抗体亲合力的结构基础”(Cryo-ET of IgG bivalent binding on SARS-CoV-2 provides structural basis for antibody avidity)的研究成果。该研究利用冷冻电子断层术(cryo-ET),系统阐明了靶向新冠病毒的IgG抗体如何双臂擒敌、协同围捕,在真实病毒囊膜表面同时锚定两个S蛋白,组装出线性或环状的高阶结构并介导病毒聚集,从而大幅提升病毒中和能力,体现出抗体通过多价结合实现对病毒的协同识别与结构性围捕。
IgG二价结合的直接结构证据
研究团队首先解析了靶向新冠病毒受体结合域的强效中和抗体P17在病毒表面的作用方式。Cryo-ET结果显示,P17-IgG可二价结合病毒囊膜上相邻的两个S蛋白,实现跨蛋白桥联。通过子断层平均法,研究团队获得了P17抗体同时结合两个S蛋白形成稳定复合物的结构细节,为IgG在天然病毒表面实现二价结合提供了直观的结构证据(图1)。
同时观察到,P17-IgG并非以单一构象发挥作用,而是在病毒表面形成多种差异化的二价结合模式。这些不同构型的S-P17-IgG双三聚体复合物可以作为基础组装单元,进一步通过二价相互作用形成高阶寡聚复合物。
IgG抗体驱动新冠病毒表面结构重排
完整新冠病毒颗粒的重构结构显示,依托P17-IgG的构象柔性和囊膜上S蛋白的动态摆动特性,P17-IgG能够募集并桥联病毒表面S蛋白,在囊膜上形成线性排布的高阶组装结构(图2),表明抗体二价结合不仅实现分子层面的桥联,还进一步驱动病毒表面蛋白的空间重组。
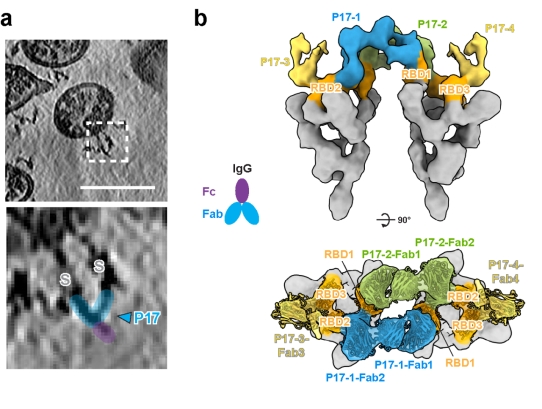
图1. P17抗体二价结合新冠S蛋白结构
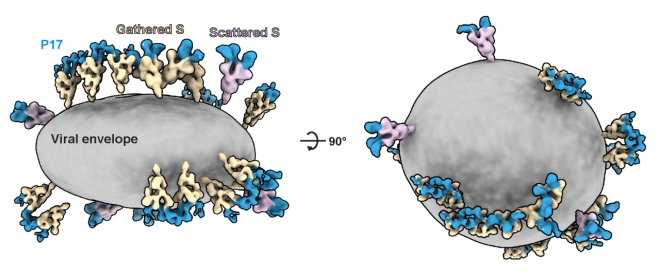
图2. P17抗体介导新冠S蛋白形成线性高阶组装
IgG的二价结合机制的普遍性验证
为验证IgG二价结合机制的普遍性,研究团队进一步分析了另一种广谱中和抗体S309。结果表明,S309-IgG亦可桥联病毒囊膜上相邻的S蛋白。与P17-IgG形成的线性高阶排布不同,S309-IgG倾向于在新冠病毒表面形成多元环状高阶复合结构,且各环状结构可进一步相互连接,在囊膜上延展形成片状排布(图3)。
值得关注的是,无论是P17-IgG诱导形成的线性高阶结构,还是S309-IgG形成的环状高阶结构,均具备免疫激活功能,可高效激活补体级联反应。这提示抗体诱导的空间排布方式可能是调控免疫效应的重要因素。
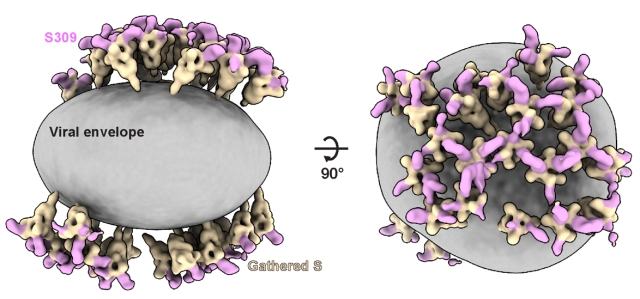
图3. S309抗体介导新冠S蛋白形成环状高阶组装
IgG抗体介导的跨病毒颗粒聚集
除在单一新冠病毒颗粒表面桥联邻近S蛋白外,更为重要的是,P17-IgG和S309-IgG均会桥联不同病毒颗粒表面的S蛋白(图4),进而介导邻近病毒颗粒发生聚集。这一现象充分体现出IgG在特定条件下促进病毒颗粒聚集的能力,尽管病毒间二价结合发生频率较低,这一作用可能增强机体对病毒的免疫识别与清除效率。
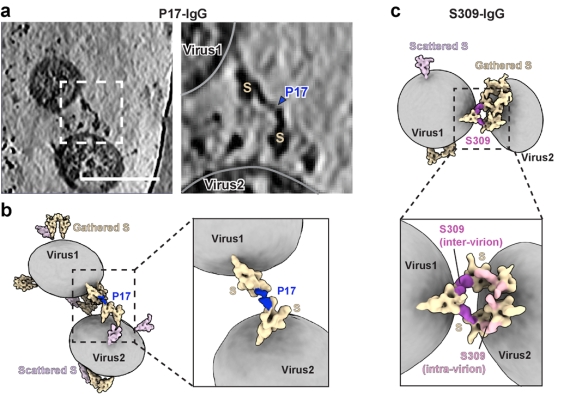
图4. P17和S309抗体介导的病毒颗粒间二价结合
功能学验证
那么,这些在囊膜病毒表面原位观测到的多价结合超级复合物,是否会增强抗体的实际中和效力?为了验证效果,研究团队对比检测了P17和S309全长IgG抗体及其Fab片段对新冠病毒的中和能力。结果显示,两种抗体的完整IgG形式中和效力均显著高于对应的Fab片段。其中,P17-IgG的半数抑制浓度(IC50)低至0.016 nM,而P17-Fab的IC50则为4.699 nM,中和效力相差近300倍!这直观证明了IgG“双臂擒敌”式二价结合在提升抗病毒效能中的巨大优势。
本团队自研FlyTomo软件
整个项目从12种样品和条件下总共解析了24个结构,最终能以两种IgG抗体、其Fab形式的对照、孵育时间梯度、抗体浓度等多个维度全面展示IgG与囊膜病毒的互作方式。这种体量的cryo-ET结构生物学必须有高性能数据处理软件支撑。
李赛课题组开发的高通量、自动化、高分辨、低门槛cryo-ET数据处理软件FlyTomo(under revision in Nat. Commun.; bioRxiv 2025)良好的满足了这种多样性异常高的原位结构解析需求。
评价
文章上线后受到同行专家的好评。新加坡国立大学的Shee-mei Lok教授评价:“这些结果可以被写进教科书,来教育学生认知IgG中和的机制(The results derived here can be included in textbooks for educating students on the mechanism of IgG neutralization)”。牛津大学的Philipp Kukura教授评价:“这些实验是我们长期以来的梦想(These are experiments we have been dreaming of for a very long time!)”
展望
本研究系统展示两种高效中和抗体P17与S309利用亲合力效应,与新冠病毒表面S蛋白实现二价结合并驱动高阶结构组装的分子机制。研究表明,IgG抗体不仅能够通过多位点结合增强与抗原的相互作用,还可调控病毒表面蛋白的空间排布,进一步放大免疫效应。本研究为阐释IgG抗体的亲合力效应构建了结构框架,并为抗体工程优化与疫苗研发提供了理论参考,尤其在优化抗原表位多聚化策略、增强免疫应答等方面具有重要价值。
生命中心、清华大学生命学院、北京生物结构前沿研究中心、膜生物学国家重点实验室李赛副教授为本研究通讯作者。浙江大学传染病诊治国家重点实验室姚航平研究员,李赛课题组宋雨桐博士、黄颀博士,浙江大学传染病诊治国家重点实验室朱淼瑾为本研究共同第一作者。李赛课题组梁佳明博士、博士生张哲源、董冬阳博士和陈勇博士参与了部分工作。
本工作得到国家自然基金委cryo-ET专项基金的支持。此外还有中国博士后科学基金,清华大学春风基金,清华大学笃实基金,生命科学联合中心、北京生物结构前沿研究中心、膜生物学国家重点实验室等支持。项目的开展离不开国家蛋白质科学研究(北京)设施清华基地冷冻电镜平台,生物计算平台和公共生物安全二级实验平台的技术支持。特别感谢雷建林博士、杨帆博士、李晓敏博士在冷冻电镜数据采集方面提供的帮助;感谢梁瑞博士和赵海帆博士惠赠实验材料。
原文链接:https://www.nature.com/articles/s41467-026-71631-5
