B 细胞是适应性免疫的重要组分,为体液免疫核心执行细胞,在抗体产生、抗原呈递及免疫调控中发挥关键作用。其活化、增殖或分化异常与自身免疫性疾病、B 细胞肿瘤等多种疾病相关。目前,靶向 B 细胞的治疗策略(如抗 CD20 抗体利妥昔单抗)已广泛应用于 B 细胞淋巴瘤、慢性淋巴细胞白血病及自身免疫性疾病等治疗。然而,迄今为止,B 细胞已知的可能的生理及病理功能均与免疫调节相关。
2026 年 4 月 17 日,生命科学联合中心/清华大学生命学院江鹏研究组在《Cell》发表题为 B-cell deficiency limits exercise capacity by remodeling liver glutamate metabolism 的研究论文。该研究揭示了 B 细胞全新的非免疫功能,鉴定出一条代谢物驱动的肝脏-骨骼肌调控通路,并提出“immunoexercise”(免疫运动) 新概念,用以描述运动能力受免疫细胞及免疫系统调控的现象。同时受到了Nature news的专访报道。
运动能力是机体健康的重要指标,依赖骨骼肌、心血管与呼吸系统协同作用。既往研究显示,运动可通过肌源性因子(myokines)调控免疫系统功能,但免疫系统对运动能力的反向调控尚无明确报道。研究人员通过基因敲除与抗体清除等方式清除或降低小鼠 B 细胞后,小鼠跑步耐力、转棒表现、自发活动及握力均显著降低,能量代谢水平下降,骨骼肌线粒体数量与结构出现损伤。上述改变未伴随体重及心脏功能的显著变化,表明运动能力下降由系统性代谢调控紊乱所致。
机制研究显示,B 细胞缺失可引发机体氨基酸代谢重编程,血清及骨骼肌谷氨酸水平显著降低。值得注意的是,该项研究的对象是免疫系统中经典的B 细胞,而非罕见的某种组织驻留亚群。进一步研究表明,B 细胞来源的 TGF-β1 减少,可下调肝脏 GLS2 和 SLC7A5 表达,重塑肝脏谷氨酸代谢,是外周谷氨酸水平降低的主要原因。骨骼肌谷氨酸水平降低可产生两方面效应:一是扰乱 Ca²⁺振荡并抑制 CaMK 信号通路,影响肌肉收缩相关信号;二是减少线粒体数量、破坏线粒体嵴结构并损伤电子传递链功能,进而系统性降低肌肉能量代谢能力。因此,谷氨酸作为关键代谢信号分子,其在肝脏与骨骼肌间的分配对维持运动能力具有重要作用。
该研究提出由 B 细胞 TGF-β1 介导的肝脏 - 骨骼肌代谢轴,可调控机体运动能力。该发现揭示了 B 细胞的免疫非依赖新功能,拓展了 B 细胞的功能范畴,为免疫系统非经典功能研究开辟了新方向;证实 B 细胞除参与免疫防御外,还可通过代谢物远程调控器官功能。该研究阐明免疫系统对运动能力的主动调控作用,更新了免疫仅受运动被动调控的传统认知。
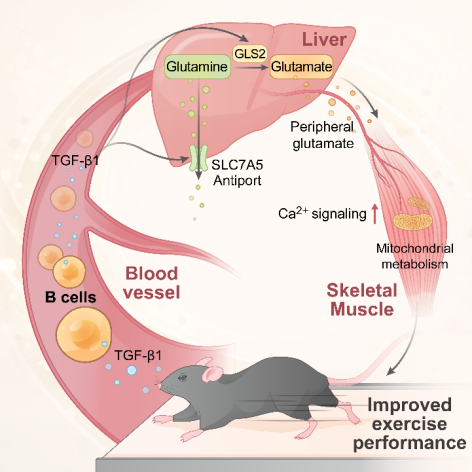
图1. B细胞非免疫依赖性调控肝脏谷氨酸代谢维持运动能力和表现。
生命科学联合中心/清华大学清华大学生命学院/江鹏副教授为本文通讯作者。清华大学生命学院在站博士后毛优翔博士、清华大学生命学院 2023 级博士研究生夏子言、清华大学基础医学院 2023 级博士研究生潘旭为共同第一作者。本项目得到生命科学联合中心、国家自然科学基金委及钱塘科学基金的资助。
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00340-5
