G蛋白偶联受体(G Protein-Coupled Receptors, GPCRs)作为人体中最大的膜蛋白超家族,广泛参与神经传导、代谢调控、免疫应答及细胞增殖等关键生理过程。据统计,全球超过30%的已上市药物以GPCR为作用靶点,其新药研发一直是GPCR研究领域的热点。稳定、高效、低成本的GPCR配体筛选方法有助于促进GPCR药物的筛选和开发。2026 年 1 月,清华-北大生命科学联合中心/清华大学药学院/北京生物结构前沿研究中心刘翔宇课题组在《细胞》(Cell) 杂志发文报道一种基于生长压力的筛选方法(Survival Pressure Selection, SPS)用于GPCR激动剂的功能性筛选(图1A)。该研究通过将GPCR信号转化为酵母生存优势,建立了低成本、高通量的激动剂筛选新策略。
在此基础上,团队进一步拓展这一筛选理念,于2026年5月13日在《细胞发现》(Cell Discovery)发表题为“A negative survival pressure selection system enables GPCR antagonist screening”的文章。该研究成功构建了一种基于“负向生存压力”的GPCR拮抗剂高通量筛选新体系(nSPS),实现了从GPCR激动剂筛选到拮抗剂筛选的技术延伸与体系完善(图1B)。依托该平台,团队鉴定出传统中药黄连和黄柏的活性成分小檗碱(Berberine)为β2肾上腺素受体(β2AR)的新型天然拮抗剂,并进一步证实其在动物模型中可有效缓解慢性压力诱导的毛发变白。该系列研究围绕“将GPCR信号转化为细胞生存压力”这一核心理念,建立了覆盖GPCR激动剂与拮抗剂筛选的功能性平台,为GPCR靶向药物的高效筛选与发现提供了新的技术工具。
以“毒性重组”实现反向筛选
GPCR在结合配体激活后,会特异性招募并偶联下游G蛋白,从而触发胞内信号级联反应。团队巧妙利用这一构象变化特征,将高毒性蛋白白喉毒素A亚基(Diphtheria toxin A, DTA)拆分为两个无活性片段,分别融合于目标GPCR的C末端与miniG蛋白中间。在未激活状态下,DTA 的两个片段在空间上彼此分离,酵母细胞可以正常增殖;当GPCR被激动剂激活并成功招募miniG蛋白时,DTA片段因空间接近而重新组装,恢复完整的ADP核糖基转移酶活性,进而抑制宿主细胞蛋白质合成,并最终导致酵母生长停滞。由于GPCR激活程度与酵母生长速率呈负相关,加入拮抗剂即可阻断G蛋白招募与DTA重组,使酵母恢复生长表型(图1C)。基于这一“受体激活即施加生存压力”的反向筛选逻辑,研究团队将该系统命名为“负向生存压力选择系统(Negative Survival Pressure Selection, nSPS)”。相比cAMP或钙流检测,nSPS无需昂贵荧光底物或探针,背景信号低,可直接以OD600为表型读出,适用于大规模天然产物库与化合物库的初筛。
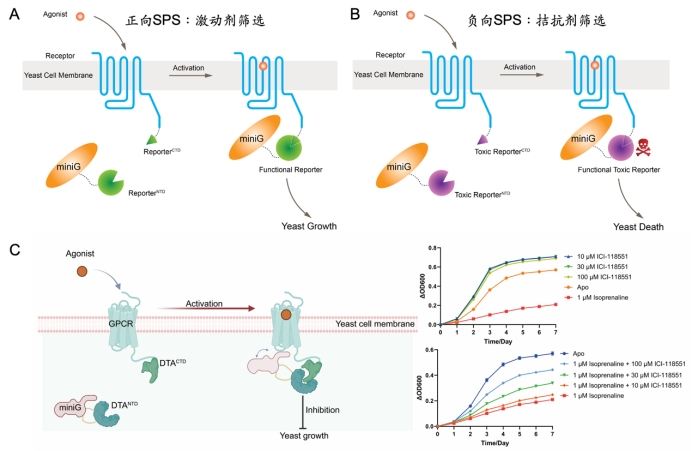
图1 SPS方法设计思路和结果。
A:正向SPS设计思路。激活GPCR促进酵母生长。该方法被成功用于筛选GPCR的新型激动剂配体(He, G. et al, Cell, 2026)。B:负向SPS(nSPS)设计思路。激活GPCR抑制酵母生长,抑制GPCR则促进酵母生长。C:毒素蛋白DTA被用于构建nSPS 系统。在培养基里存在受体激动剂时,酵母生长缓慢;而在培养基里加入受体拮抗剂时,酵母快速生长。
nSPS方法助力发现小檗碱为β2AR拮抗剂,具有治疗压力型白发的潜力
依托nSPS平台,研究团队以β2AR为模式受体,对包含约一千种天然产物的化合物库进行高通量筛选。经后续细胞实验验证,团队成功鉴定出去亚甲基小檗碱(Demethyleneberberine)及其类似物小檗碱(Berberine)为β2AR的新型拮抗剂。为进一步揭示其分子作用机制,团队利用单颗粒冷冻电镜技术成功解析了β2AR 结合小檗碱复合物的高分辨率结构。结构分析表明,小檗碱结合在β2AR的正构结合口袋(图2),但其结合取向与空间占据模式与经典合成拮抗剂存在差异。突变实验进一步验证了该结合模式。
近年多项研究揭示,慢性心理或生理压力可激活交感神经系统,促使去甲肾上腺素大量释放,过度激活毛囊微环境中的β2AR,进而导致黑色素干细胞不可逆耗竭,引发毛发加速变白。阻断该通路被视为干预“压力性白发”的潜在策略。小檗碱作为传统中药黄连、黄柏等药材中的核心活性生物碱,在东亚传统医学中已有数千年应用历史,其安全性及体内代谢特征已得到较充分验证。研究团队利用压力诱导毛发变白小鼠模型,发现外用小檗碱可以有效延缓压力诱导的毛发变白。该研究揭示了小檗碱这一传统中药活性成分在毛发健康领域的全新应用潜力(图2)。
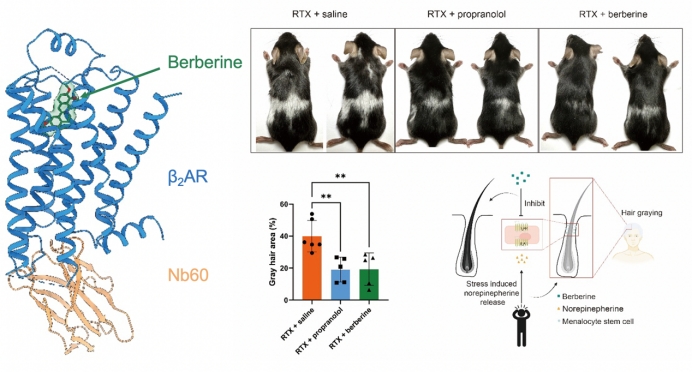
图2 小檗碱结合在β2AR正构口袋(左),且在压力诱导的毛发变白小鼠模型中表现出治疗效果(右)。
nSPS 平台可应用于不同GPCR
为全面评估nSPS系统的通用性,研究团队进一步将其拓展至两类不同的GPCR靶点:一类是内源性配体为多肽的黑素皮质素受体5(MC5R),另一类则是主要偶联Gq蛋白的孤儿受体GPR39。凭借其模块化设计以及可直接通过酵母生长表型进行筛选的优势,nSPS系统成功实现了MC5R的高通量拮抗剂筛选,并意外发现原本用于抑制RAS肿瘤信号通路的小分子Pan-RAS-IN-1可作为MC5R的新型拮抗剂;同时,团队也在GPR39 体系中也建立了稳定的信号窗口,证明该系统可兼容Gs、Gq等不同G蛋白亚型偶联偏好的 GPCR。这一系列结果表明,nSPS可发展成通用化的GPCR拮抗剂筛选平台。
结语与展望
综上所述,刘翔宇团队自主研发的nSPS筛选平台为GPCR拮抗剂药物发现提供了一条高效、通用、低成本的新路径。同时,本研究还展示了传统中药活性成分在现代受体药理学中的巨大开发价值。
生命中心/清华大学药学院刘翔宇课题组博士生徐涛和孙沁心为本研究的第一作者。深圳儿童医院刘中杰博士、北京美慕科技有限公司王娟博士、刘翔宇课题组何国栋博士以及刘翔宇副教授为本研究通讯作者。刘翔宇课题组原成员张书豪博士(现为斯坦福大学博士后),孙晓鸥博士以及北京美慕科技有限公司刘婷竹为研究做出了重要贡献。中山大学王旭升教授为动物实验提供了重要指导。沈阳药科大学无涯创新学院林斌教授在分子动力学模拟方面提供了重要帮助。本研究得到了国家自然科学基金委,北京生物结构前沿研究中心,清华-北大生命科学联合中心以及清华大学“笃实专项”的资助。国家蛋白质科学中心(北京)清华大学分中心冷冻电镜平台,清华大学药学技术中心,清华大学同位素实验室和北京水木未来生物科技公司为本研究提供了重要技术支持。本研究使用的 NanoBiT 系统相关质粒由日本京都大学/东北大学Asuka Inoue 教授馈赠。
原文链接:
https://www.nature.com/articles/s41421-026-00892-7
